ORIGINALARBEIT
Trockenvernebelung von Peroxyessigsäure: Ein universelles viruzides, bakterizides und sporozides Raumdesinfektionsverfahren?
Dry fogging of peroxyacetic acid: a universal virucidal, bactericidal and sporicidal procedure for room disinfection?
Sven Reichea, Jan Schinköthea, Sandra Diedericha, Hendrik Scheinemanna, Michael Eschbaumera, Holger Freesea, Kathrin Klugeb, Jens P. Teifkea
a Friedrich-Loeffler-Institut, Bundesforschungsinstitut für Tiergesundheit, Greifswald-Insel Riems
b Wehrwissenschaftliches Institut für Schutztechnologien ABC-Schutz, Munster
Zusammenfassung
Zur Verhinderung einer Freisetzung von Biostoffen müssen mikrobiologische Laboratorien technische Verfahren und praktische Verfahrensweisen anwenden, um Arbeitsflächen, Schutzausrüstung, Gegenstände und Räume innerhalb der Sicherheitsbereiche wirksam zu dekontaminieren. Außerhalb der Infektionsforschung sind die biologische Dekontamination im medizinischen Bereich (z. B. Sonderisolierstationen, Rettungsdienstfahrzeuge), in der Landwirtschaft (z. B. Tierställe und Transportfahrzeuge) sowie bei der Prävention und Kontrolle von Infektionskrankheiten bei Mensch und Tier von größter Bedeutung.
Unter Dekontamination werden Prozesse der Reinigung, Desinfektion und Sterilisation zusammengefasst, die letztlich Biostoffe auf ein gesundheitlich unbedenkliches Maß reduzieren. Die ultrafeine Vernebelung von Desinfektionsmitteln als Aerosol geringer Partikelgröße (~7,5 µm) gelingt durch den Venturi-Effekt bei Verwendung einer Aerosoldüse unter Anwendung von Druckluft. Solch ein „trockener Nebel“ (engl. dry fog) kann sich als Aerosol bei nur minimaler Kondensation auf Oberflächen lange in der Schwebephase halten. Aufgrund der über einen weiten Temperaturbereich bestehenden breiten mikrobiziden Eigenschaften eignet sich besonders Peroxyessigsäure (PES) für Infrastrukturdekontaminationen. Dabei können durch die trockene Feinvernebelung die korrosiven Eigenschaften der PES weitestgehend vermieden werden. Abhängig von der relativen Luftfeuchtigkeit und der Temperatur kann unter optimalen Bedingungen eine Keimreduktion um sechs Größenordnungen (106) für Viren, vegetative Bakterien und Sporen erzielt werden. Dies erklärt, warum „Dry Fogging“ bereits erfolgreich in der Reinraumtechnologie und zur Desinfektion von Operationssälen und am Friedrich-Loeffler-Institut für die Dekontamination zum „Shutdown“ der S4-Laboratorien und Tierräume eingesetzt wird.
Schlüsselwörter: Dekontamination, Desinfektion, Peroxyessigsäure, Bioindikator, Aerosol, Viren, Bakterien, Sporen.
Summary
In order to prevent the release of biological agents, microbiological laboratories must apply technical procedures and practical methods to decontaminate work surfaces, protective equipment, objects and rooms within the containment areas effectively. Apart from infectious disease research, biological decontamination is of utmost importance in the medical sector (e.g. special isolation wards, rescue service vehicles), in agriculture (e.g. animal facilities and transport vehicles) and in the prevention and control of infectious diseases in humans and animals.
The term decontamination refers to processes of cleaning, disinfection and sterilization, which ultimately reduce biological agents to a level that is harmless to health. The ultra-fine nebulization of disinfectants as an aerosol of small particle size (~ 7.5 µm) is achieved by the “Venturi effect” when forcing compressed air through an aerosol nozzle. Such a dry fog can remain in suspension for a long time as an aerosol, with only minimal condensation on surfaces. Due to its broad microbicidal properties over a wide temperature range, peroxyacetic acid (PAA) is particularly suitable for infrastructure decontamination. The corrosive properties of PAA can be minimized by ultra-fine aerosolization. Depending on the relative humidity and temperature, a germ reduction of six orders of magnitude (106) for viruses, vegetative bacteria and spores is achieved. This explains why dry fogging has been applied successfully in clean room technology and for the disinfection of operating rooms and at the Friedrich-Loeffler-Institut for decontamination of S4 laboratories and animal rooms in preparation for their shutdown.
Keywords: decontamination, disinfection, peroxyacetic acid, bioindicator, aerosol, viruses, bacteria, spores.
Einleitung
Die Dekontamination von biologisch kontaminierter Infrastruktur im Zusammenhang mit hochkontagiösen Infektionskrankheiten bei Menschen und Tieren oder bei bioterroristischen Gefahrenlagen ist im Sinne des „One-Health“-Konzeptes von zentraler Bedeutung für Bevölkerung, Tier- und Umwelt. Solche zu dekontaminierenden Räumlichkeiten finden sich unter anderem bei Sonderisolierstationen der Patientenversorgung, Fahrzeugen im Rettungsdienst, Verkehrsmitteln zum Personen-, Tier- und Warentransport, militärischen Fahrzeugen und Geräten, insbesondere bei der Rückverlagerung aus Einsatzgebieten. Gerade bei dem Abzug großer militärischer Kontingente aus Regionen mit endemischen Tierseuchenerregern muss eine Verschleppung dieser teils auch zoonotischen Pathogene ausgeschlossen werden.
Für den Betrieb und insbesondere für die Notfallplanung bei nicht bestimmungsgemäßen Betriebszuständen von Hochsicherheitsbereichen hat die Dekontamination der Laborräume, in denen Tätigkeiten unter hohen Sicherheitsbedingungen nach Biostoffverordnung, Infektionsschutzgesetz, Gentechnik- oder Tierseuchenrecht ausgeführt werden, einen besonderen Stellenwert. Fast immer erfolgt dies fallbezogen, je nach den beteiligten Biostoffen sowie möglichen Expositionsszenarien und auf der Grundlage von zuvor durchgeführten Gefährdungsbeurteilungen. Hierfür kommen entweder nass-chemische Behandlungen sämtlicher Oberflächen oder – nach erfolgter gründlicher Vorreinigung – auch Gas- oder Aerosoldesinfektionsverfahren zum Einsatz. Dabei werden Oberflächen und Geräte in einem abdichtbaren Raum durch gasförmiges Formaldehyd, verdampftes Wasserstoffperoxid [16] oder vernebelte PES behandelt. Der Vorteil dieser Desinfektionsverfahren ist darin begründet, dass auch schlecht zugängliche und damit schwierig benetzbare Bereiche durch die Desinfektionsmittel wirksam erreicht werden können [20]. Somit wird der Raum mit den darin befindlichen Gegenständen (z. B. elektrische Installationen, Laborausstattung, hochwertige Laborgeräte) desinfiziert, die häufig nicht autoklavierbar sind und nicht nasschemisch behandelt werden können.
Allen diesen Raumdesinfektionsverfahren gemeinsam ist die vorherige teils aufwändige Etablierungs- und Validierungsphase. Aktuelle Publikationen belegen für PES die Inaktivierung von Viren, Bakterien und Sporen [6][8]. Hingegen fehlen noch Wirksamkeitsnachweise für veterinärmedizinisch bedeutsame Erreger wie das Maul- und Klauenseuchevirus, Mycobacterium sp. und Bacillus (B.) anthracis.
Gas- und Aerosoldesinfektionsverfahren
Falls eine Oberflächenwischdesinfektion, deren Standardisierung darüber hinaus nur sehr schwierig möglich ist [7], nicht ausreichend ist, sind Raumbegasungen oder Vernebelungen zu bevorzugen [18]. Verschiedene primäre und sekundäre Faktoren beeinflussen dabei grundsätzlich die Wirksamkeit der Desinfektion. Dazu gehören
- die Menge und Art der Mikroorganismen,
- das Vorhandensein von organischer Matrix,
- Menge, Art, Konzentration und Einwirkzeit des Desinfektionsmittels sowie
- der Reinheitsgrad, Art und Beschaffenheit der zu desinfizierenden Oberflächen.
Die wichtigsten umweltassoziierten Faktoren sind die Raum- bzw. Einwirktemperatur sowie die relative Luftfeuchtigkeit (rH) und Luftgeschwindigkeit [10][17][20]. Bedeutsam bei der Auswahl des Desinfektionsmittels ist seine Materialverträglichkeit. Am wichtigsten hierbei sind die Konzentration des Desinfektionsmittels und seine Einwirkzeit. Diese Faktoren korrelieren meist umgekehrt proportional miteinander [5].
Die Verwendung der meisten mikrobiziden Gase wie Ethylenoxid und Formaldehyd ist durch die Bestimmungen des Chemikaliengesetzes und der Gefahrstoffverordnung erlaubnispflichtig und für den Durchführenden mit entsprechenden Sachkundenachweisen gekoppelt. Dabei sind auch die Bestimmungen der Technischen Regeln für Gase (z. B. TRGS 522) zu beachten [20].
Formaldehyd
Formaldehydbegasungen werden seit mehr als einhundert Jahren für die Flächendesinfektion verwendet und nehmen auch heute noch international eine führende Position bei der Dekontamination von Hochsicherheitslabor- oder Schleusenräumen, empfindlicher Geräteausstattung, „high efficiency particulate air“ (HEPA)-Filtern und ihrer Gehäuse, mikrobiologischen Sicherheitswerkbänken sowie Tierräumen und Käfigen ein [1][4][10]. Neben den niedrigen Kosten und den sehr einfach zu bedienenden und robusten Begasungsapparaturen begründet vor allem die bewiesene Wirksamkeit gegenüber einer großen Breite an Erregern die langjährige Popularität der Formaldehydbegasung. Allerdings muss in den meisten Fällen nach einer Kontaktzeit von üblicherweise 12 Stunden Formaldehyd mittels Ammoniak neutralisiert werden. Die daraus entstehenden Methenamin-Nebenprodukte bilden als Nachteil einen weißen Niederschlag, der aufwändig durch Wischreinigung entfernt werden muss [3][10].
Die mikrobizide Aktivität von Formaldehyd beruht auf der sehr reaktiven Aldehydgruppe, die vor allem mit den Amino- und Amidgruppen der Zellproteine reagiert und irreversible Methylgruppen ausbildet. Die daraus resultierende Quervernetzung von mikrobiellen Proteinen mit Nukleinsäuren führt zu einer Inaktivierung des Biostoffes. Dies begründet aber auch den hohen Eiweißfehler der Aldehyde [1][9][20]. Die am wenigsten empfindlichen Organismen gegenüber Formaldehyd sind die Sporen von Bacillus spp. sowie Geobacillus (G.) stearothermophilus [10][17]. Aus diesem Grunde werden für die Validierung der Formaldehydbegasung als biologische Indikatoren am häufigsten Sporen des B. atrophaeus (B. subtilis) bzw. des G. stearothermophilus verwendet [4].
Alternativen zu Formaldehyd
Trotz zahlreicher Vorteile gibt es bei Formaldehyd auch nicht unerhebliche Nachteile, die insbesondere auf seiner Toxizität und Kanzerogenität beruhen. Seit geraumer Zeit werden deshalb Alternativen zur Raumbegasung mit Formaldehyd gesucht. In Anwendung sind aktuell verdampftes Wasserstoffperoxid (H2O2), gasförmiges Chlordioxid (ClO2), Ethylenoxid oder vernebelte PES. Allen Verfahren gemein ist ihre reduzierte Wirksamkeit bei hoher organischer Grundbelastung, beispielsweise durch Blut- oder Kotverschmutzung. Kontaminierte Areale müssen deshalb – und dies ist kein neues Prinzip wirksamer Dekontaminationsmaßnahmen – zunächst gründlich oberflächengereinigt werden [20].
Peroxyessigsäure
Die PES oder exakter Peroxyessigsäure (C2H4O3) enthält zur Stabilisierung Wasserstoffperoxid und Essigsäure im Überschuss. Maximal können in der Lösung ca. 46 % PES erreicht werden. Bereits in den 1960er Jahren gab es erste Versuche, fein vernebelte PES bei einer rH von 80 % anzuwenden, um Sporen von B. atrophaeus auf Keimträgern aus Papier oder Glas zu inaktivieren [14]. Als viruzide Konzentration haben sich in nasschemischen Verfahren 0,002 % bis 0,225 % PES gegenüber einer Reihe von behüllten und unbehüllten Viren als wirksam erwiesen [2]. Was die Materialverträglichkeit betrifft, sind Aluminium, Edelstahl, sowie verzinntes Eisen resistent, während Stahl, galvanisiertes Eisen, Kupfer und Messing korrosionsempfindlich sind [19]. Durch trockene Feinvernebelung und der Wirksamkeit bei geringen Konzentrationen können die korrosiven Wirkungen der PES jedoch vermieden werden. Im Jahr 2001 wurde ein automatisiertes Vernebelungs-Desinfektionsverfahren, das „Dry fogging system“ von der Firma Ikeuchi Co., Ltd., Osaka, Japan [11] zur Desinfektion von Operationssälen entwickelt [Übersichtbei8].
Im Folgenden wird über die Validierung des Verfahrens für drei unterschiedliche Räume zwischen 245 m3 und 675 m3 Rauminhalt sowie die experimentell erzielten Ergebnisse berichtet, die bei Verwendung unterschiedlicher Keimträger für behüllte und unbehüllte Viren sowie Mykobakterien und bakterielle Sporen erhalten wurden.
Methoden
Desinfektionsmittel, -equipment und -zyklus
Als Desinfektionsmittel wurde das Minncare Sterilant (MarCor, Heerlen, Niederlande) mit demineralisiertem Wasser auf die gewünschte PES-Wirkstoffkonzentration verdünnt. Der jeweilige Desinfektionszyklus bestand aus einer Trockenvernebelungsphase, in der die benötigte Menge an Desinfektionsmittel solange ausgebracht wurde, bis an allen Messstellen die gewünschte rH (90 bis 99 %) erreicht wurde. Dem folgte eine Einwirkzeit von 30 min bzw. 180 min. Den Abschluss der Desinfektionsmaßnahme bildete eine Belüftungszeit von 30 min. Der Betrieb des Trockenvernebelungsgerätes „Dry Fog 2S“ (MarCor) fand mit 3 bar Druckluft bei mindestens 70 l/min Luftförderleistung je verwendeter Düse statt, die von ölfrei laufenden Kompressoren erzeugt wurde.
Testräume und Zyklusparameter
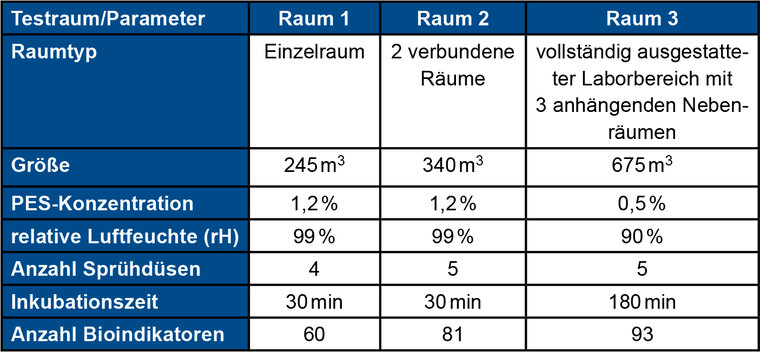
Die Beschreibung der Testräume und der -parameter ist Tabelle 1 zu entnehmen.
Tab. 1: Testräume und -parameter
Bioindikatoren
Zum spezifischen Wirksamkeitsnachweis wurden Keimträger als Bioindikatoren (BI) mit ausgewählten viralen und bakteriellen Erregern präpariert und ausgebracht. Hierzu fanden rechteckige 16x60 mm große Keimträger aus Edelstahl der Qualität 2B nach EN 10088-2 (GK Formblech GmbH, Berlin) in Übereinstimmung mit der Leitlinie der Deutschen Vereinigung zur Bekämpfung der Viruskrankheiten (DVV) Verwendung [15].
Getestete Bakterien
Zur Inaktivierung wurden folgende Bakterien getestet: Je 50 µl Virus-, Bakterien- bzw. Sporensuspension wurden auf den Keimträgern im Ausstrichverfahren ausgebracht (10 µl/cm²) und für 30-60 min in einer Werkbank getrocknet. Des Weiteren kamen Sporen von B. subtilis (BS) und G. stearothermophilus (ATCC 12980, GS) zur Verwendung. Als weniger virulentes Surrogat für Mycobacterium (M.) tuberculosis wurde M. senegalense (MS) (DSM 110653)eingesetzt.
Getestete Viren
Folgende Viren wurden ebenfalls als BI getestet: Murines Norovirus (MNV), Familie Caliciviridae, ist ein unbehülltes RNA-Virus, das in der Desinfektionsmittelprüfung standardisiert eingesetzt wird und damit als Surrogaterreger für das ebenfalls unbehüllte Maul- und Klauenseuchevirus (MKSV) aus der Familie der Picornaviridae dienen kann. Als Erreger der anzeigepflichtigen Maul- und Klauenseuche ist es von enormer volkswirtschaftlicher Bedeutung. Das Virus der Stomatitis vesicularis Typ Indiana (VSV) ist ein behülltes Virus der Rhabdoviridae, das als Surrogaterreger für hochpathogene hämorrhagische Fieberviren der Risikogruppe 4, wie Ebolavirus oder Lassa-Virus verwendet wird.
Probengewinnung
Der mit PES behandelte BI wurde nach dem Ende der Vernebelung mit Nährmedium abgespült, in Zehnerschritten verdünnt und unter geeigneten Bedingungen inkubiert. Im Falle von BS und MS erfolgte eine 7-tägige Inkubation bei 37 °C, für GS bei 60 °C. Die Viren wurden in Zehnerschritten verdünnt und auf geeigneten Zelllinien im Brutschrank bei 37 °C und 90 % Luftfeuchtigkeit und 5 % CO2 kultiviert.
Auswertung und Kontrollen
Die Auswertung der einzelnen Verdünnungsstufen geschah dabei qualitativ:
- Bakterienwachstum, gekennzeichnet durch Trübung oder Verfärbung des Nährmediums (positiv) sowie
- im Falle von Viren durch das Auftreten von zytopathischen Effekten der Zellen (positiv),
- bei Fehlen dieser Veränderungen (negativ).
Jeweils ein BI verblieb während der Vernebelung in einer dichtverschlossenen Plastikbox unbehandelt und diente als Referenz zur Bestimmung des vorhandenen Virustiters oder der Keimzahl. Ebenso wurden Toxizitätskontrollen entsprechend der DVV-Leitlinie mitgeführt [15].
Ergebnisse und Diskussion
Mit dem hier beschriebenen Trockenvernebelungsverfahren können Partikel mit einem mittleren massenbezogenen medianen aerodynamischen Durchmesser von ≤ 7,5 µm generiert werden. Es entsteht ein ultrafeines Aerosol, das sich im beaufschlagten Raum gleichmäßig verteilt. Des Weiteren verbleiben diese Tröpfchen auf Grund ihrer geringen Größe über mehrere Stunden in der Schwebephase [12] und sedimentieren erst spät auf waagerechten Oberflächen. Selbst Räume mit komplexer Gebäudetechnik lassen sich auf diese Weise behandeln (Abbildungen 1a und 1b).

Abb. 1: Durch das Trockenvernebelungsverfahren wird ein ultrafeiner Peroxyessigsäurenebel generiert, der es erlaubt, bei guter Materialverträglichkeit auch komplexe Technikräume von ca. 500 m3 durch Aerosol zu desinfizieren.
(a) Zu Beginn des Desinfektionszyklus sieht man das Austreten des Nebels aus den Vernebelungsdüsen des Nebelgenerators (Pfeil).
(b) Nach Abschluss der ca. 15 min Ausbringungsphase herrscht während der Einwirkzeit ein dichter trockener Nebel.
Für den Nachweis der bioziden Wirkung des Verfahrens wurden drei Räume ausgewählt, in denen die unterschiedlichen vorbereiteten Bioindikatoren ausgebracht wurden. Dabei wurden insgesamt zwei unterschiedliche Zyklusprogramme getestet. Im Programm 1 wurde eine höhere PES-Konzentration von 1,2 % und auch eine höhere rH von mindestens 99 % an allen Messpunkten im Raum angestrebt. Die Inkubationszeit betrug nach dem Erreichen der geforderten Luftfeuchte 30 min. Bei den mit diesen Parametern behandelten Räumen 1 und 2 handelte es sich um Tierhaltungs- bzw. Sektionsräume.
Daneben kam auch noch ein vollständig ausgestatteter Laborraum (Raum 3) als Testobjekt zum Einsatz. Um die Materialschonung des Verfahrens noch weiter zu erhöhen, wurde die verwendete PES-Konzentration hier auf 0,5 % reduziert. Gleiches galt für die rH, welche diesmal einen Maximalwert von 90 % nicht überschreiten sollte. Um die vorgenommenen Reduktionen der Wirkstoffkonzentration sowie der relativen Luftfeuchte zu kompensieren, wurde die Inkubationszeit auf 180 min erhöht.
Unter Verwendung der beiden unterschiedlichen Parameter konnten in allen drei Testräumen für alle ausgebrachten Keimträger mit den verschiedenen Bioindikatoren eine Reduktion von mindestens 5 Log-Stufen erzielt werden (Abbildung 2).
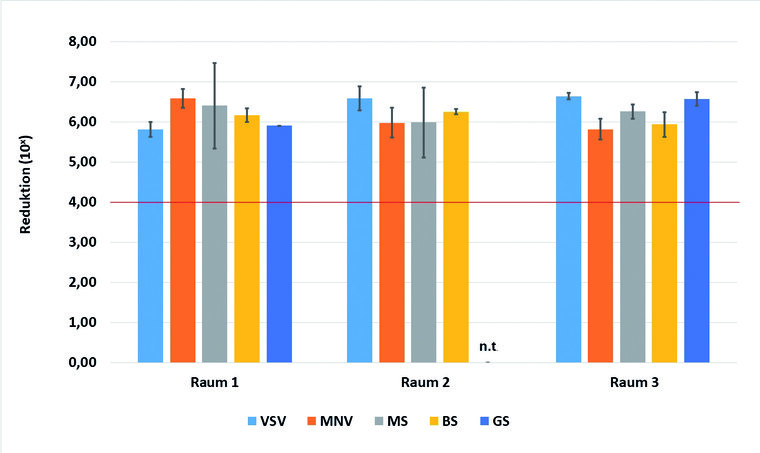
Abb. 2: Erzielte Reduktion der verwendeten Bioindikatoren (VSV: Virus der Stomatitis vesicularis; MNV: Murines Norovirus; MS: Mycobacterium senegalense; BS: Bacillus subtilis; GS: Geobacillus stearothermophilus) in den drei unterschiedlichen Testräumen; dargestellt sind die erzielten Reduktionen aller ausgebrachten BI als Mittelwerte mit Standardabweichung.
Die Anforderungen „Desinfektion“ nach OENORM EN 17272:2018-09-01 sind als rote Linie dargestellt.
Für diese effektive Inaktivierungswirkung der PES-Trockenvernebelung sollte dabei die Ausgangsluftfeuchtigkeit nicht weniger als 45 % und nicht mehr als 60 % rH betragen.
Darüber hinaus wurde gezeigt, dass eine Steigerung der Inaktivierungseffizienz der trockenvernebelten Peroxyessigsäure auch durch eine Wiederholung des gesamten Inaktivierungszyklus erzielt werden kann. Bei den beiden verwendeten Prozessparametern konnten auf behandelten Oberflächen und dem zusätzlich mitgeführten technischen sowie auch elektronischen Equipment keine sichtbaren und funktionellen Schäden beobachtet werden.
Abschließende Bewertung
Unsere Untersuchungen haben gezeigt, dass sich die hier beschriebene Methode, unter Einhaltung der hier getesteten Prozessparameter, zur effizienten Abschlussdesinfektion gegenüber einem großen Erregerspektrum vorgereinigter Räumlichkeiten eignet. Es ist in diesem Kontext erwähnenswert, dass die Autoren der RKI-Richtlinie bereits im Jahr 1994 betreffs der Festlegungen zur Beschichtung von Keimträgern für die Flüssigdesinfektion von Oberflächen folgendes festhielten:
„Wir glauben, damit einen Kompromiss gefunden zu haben, zwischen dem Bestreben, einerseits mit der Prüfmethodik merklich kontaminierte Flächen zu erfassen, und dem Bestreben bei der Flächendesinfektion nur eine sehr begrenzte Desinfektionsmittelmenge pro kontaminierter Fläche einzusetzen. Deshalb ist die Flächendesinfektion nicht zur Desinfektion grob verschmutzter Flächen geeignet“ [13].
Bei der Trockenvernebelung ist insbesondere die Desinfektionsmittelmenge im Verhältnis zur kontaminierten Fläche um Größenordnungen geringer als bei einer Wischdesinfektion, sodass die Aussagen der RKI-Richtlinie erst recht für eine Raumdekontamination unter Verwendung von aerogenen Desinfektionsverfahren gelten.
Fazit
Die Anwendung einfach zu handhabender und sicher wirksamer Verfahren zur Raum- und Flächendesinfektion ist – auch vor dem Hintergrund der COVID-19-Pandemie – sowohl für Krankenhäuser als auch für mobile Einrichtungen des Sanitätsdienstes von wehrmedizinischer Relevanz. Mit der PES-Trockenvernebelung steht ein solches auch als Alternative zur Formaldehydbegasung zur Verfügung.
Kernsätze
- Die Desinfektion biologisch kontaminierter Räume ist ein zentrales Thema der Infektionsmedizin, Tierseuchenbekämpfung und mikrobiologischer Laboratorien.
- Raumdesinfektion durch Aerosol-gestützte Vernebelungsverfahren ist der nasschemischen Dekontamination überlegen, weil eine längere Einwirkzeit der gleichmäßig verteilten Desinfektionsmittel auch in schlecht zugänglichen Bereichen möglich ist.
- Die Trockenvernebelung von Peroxyessigsäure (PES) erweist sich als geeignetes Desinfektionsverfahren auch größerer und komplexer Räume von mehr als 500 m3 Volumen.
- Die trockenvernebelte PES reduziert die Keimzahl auf Bioindikatoren um mindestens 5 Log-Stufen im Falle behüllter und unbehüllter Viren, Mykobakterien und Sporen.
Literatur
- Abraham G: Formaldehyde fumigation for BSL-3 facilities. In J. Y. Richmond (Ed.), Anthology of biosafety VII: Biosafety level 3. Mundelein, IL 2004: American Biological Safety Association. mehr lesen
- Block SS: Disinfection, sterilization, and preservation. 2001: Lippincott Williams & Wilkins. mehr lesen
- Czarneski MA: Selecting the right chemical agent for decontamination of rooms and chambers. Appl Biosaf 2007; 12(2): 85-92. mehr lesen
- Gordon D, Madden B, Krishnan J, Klassen S, Dalmasso J, Theriault S: Implications of paper vs stainless steel biological indicator substrates for formaldehyde gas decontamination. J Appl Microbiol 2011; 110(2): 455-462. mehr lesen
- Gordon D, Carruthers B-A, Theriault S: Gaseous Decontamination Methods in High-containment Laboratories. Appl Biosaf 2012; 17(1): 31-39. mehr lesen
- Gregersen J-P, Diebold T, Roth B: Virusinaktivierung mit vernebelter Peressigsäure. Hyg Med 2013; 38(6): 238-244.
- Krause J, McDonnell G, Riedesel H: Biodecontamination of animal rooms and heat-sensitive equipment with vaporized hydrogen peroxide. Contemporary Topics in Laboratory Animal Science/American Association for Laboratory Animal Science 2001; 40: 18-21. mehr lesen
- Krishnan J, Fey G, Stansfield C et al.: Evaluation of a Dry Fogging System for Laboratory Decontamination. Appl Biosaf 2012; 17(3):1 32-141. mehr lesen
- Loshon CA, Genest PC, Setlow B, Setlow P: Formaldehyde kills spores of Bacillus subtilis by DNA damage and small, acid-soluble spore proteins of the alpha/beta-type protect spores against this DNA damage. J Appl Microbiol 1999; 87: 8-14. mehr lesen
- Munro K, Lanser J, Flower R: A comparative study of methods to validate formaldehyde decontamination of biological safety cabinets. Appl Environ Microbiol 1999; 65(2): 873-876. mehr lesen
- Nakata S, Ikeda T, Nakatani H et al.: Evaluation of an automatic fogging disinfection unit. Env Health Prev Med 2001; 6(3): 160-164. mehr lesen
- Nicas M, Nazaroff WW, Hubbard A: Toward understanding the risk of secondary airborne infection: emission of respirable pathogens. J Occup Environ Hyg 2005; 2(3): 143-54. mehr lesen
- Peters J: Richtlinie des Bundesgesundheitsamtes zur Prüfung der Wirksamkeit von Flächendesinfektionsmitteln für die Desinfektion bei Tuberkulose. Bundesgesundheitsbl 1994; 37: 274–278. mehr lesen
- Portner DM, Hoffman RK: Sporicidal effect of peracetic acid vapor. Appl Microbiol 1968; 16(11): 1782-1785. mehr lesen
- Rabenau HF, Schwebke I, Steinmann J, Eggers M, Rapp I, Neumann-Haefelin D: Quantitative Prüfung der viruziden Wirksamkeit chemischer Desinfektionsmittel auf nicht-porösen Oberflächen. Hyg Med 2012; 37: 78-85. mehr lesen
- Reichenbacher D, Thanheiser M, Krüger D: Aktueller Stand zur Raumdekontamination mit gasförmigem Wasserstoffperoxid. Hyg Med 2010; 35 [6]: 204-208. mehr lesen
- Rogers J, Choi Y, Richter W, Rudnicki D et al.: Formaldehyde gas inactivation of Bacillus anthracis, Bacillus subtilis, and Geobacillus stearothermophilus spores on indoor surface materials. J Appl Microbiol 2007; 103(4): 1104-1112. mehr lesen
- Rogers JV, Choi YW, Richter WR, Stone HJ, Taylor ML: Bacillus anthracis spore inactivation by fumigant decontamination. Appl Biosaf 2008; 13(2): 89-98. mehr lesen
- Schröder W: Peracetic acid: Disinfectant for the food industry. Nürnberg: Brauwelt International 1984; 1: 118-120.
- Strauch D, Böhm R: Reinigung und Desinfektion in der Nutztierhaltung und Veredelungswirtschaft. 2002: Enke. mehr lesen
Erklärung zum Interessenkonflikt und zur Finanzierung:
Die Autoren erklären, dass kein Interessenkonflikt besteht. Das Forschungsvorhaben wurde durch das Bundesministerium der Verteidigung, Zuwendungsbescheid: E/E590/FZ005/FF005 / interne Bezeichnung Ri-0381, vollfinanziert.
Manuskriptdaten
Eingereicht: 16. April 2020
Angenommen: 11. Mai 2020
Zitierweise
Reiche S, Schinköthe J, Diederich S, Scheinemann H, Eschbaumer M, Freese H, Kluge K, Teifke JP: Trockenvernebelung von Peroxyessigsäure: Ein universelles viruzides, bakterizides und sporozides Raumdesinfektionsverfahren? WMM 2020; 64(10-11): 370-375.
Für die Verfasser
Oberstveterinär d. R. Prof. Dr. Jens Peter Teifke
Friedrich-Loeffler-Institut, Bundesforschungsinstitut für Tiergesundheit
Abteilung für experimentelle Tierhaltung und Biosicherheit
Südufer 10, 17493 Greifswald-Insel Riems
E-Mail: jenspeter.teifke@fli.de
Manuscript data
Submitted: 16 April 2020
Accepted: 11 May 2020
Citation
Reiche S, Schinköthe J, Diederich S, Scheinemann H, Eschbaumer M, Freese H, Kluge K, Teifke JP: Dry fogging of peroxyacetic acid: a universal virucidal, bactericidal and sporicidal procedure for room disinfection? WMM 2020; 64(10-11): 370-375.
For the authors
Colonel (Reserve) Prof. Dr. Jens Peter Teifke
Friedrich-Loeffler-Institut, Federal Research Institute for Animal Health
Department of Experimental Animal Facilities and Biorisk Management
Suedufer 10, 17493 Greifswald-Insel Riems
E-Mail: jenspeter.teifke@fli.de