DES PUDELS KERN
Radiologische oder nukleare Katastrophen –
wie darauf vorbereiten?
Matthias Porta, Michael Abenda
aInstitut für Radiobiologie der Bundeswehr, München
Zusammenhänge und Szenarien
„Auf dem Spaziergang begibt sich ein schwarzer Pudel an Fausts Seite, der ihn bis in sein Studierzimmer begleitet. Vor seinen Augen verwandelt sich das Tier in Mephisto und Faust ruft erstaunt aus: „Das also war des Pudels Kern.“
Noch heute wird der Ausdruck „Des Pudels Kern“ verwendet, um auf den wesentlichen Punkt einer Sache hinzuweisen. Und genau hier setzt das Institut für Radiobiologie der Bundeswehr (InstRadBioBw) mit seiner Problemanalyse zum Medizinischen A-Schutz an:
- Strahlenexposition mit hohen Dosen führt innerhalb von Sekundenbruchteilen zu starken Zellschäden und zeitverzögert zu massivem Zelltod und damit assoziierten Organfunktionsverlusten.
- Die lebensgefährliche Akute Strahlenkrankheit (ASK) manifestiert sich erst Tage oder Wochen nach Bestrahlung – viel Zeit, um zu reagieren.
- Was ist die entscheidende diagnostische Fragestellung in dieser Situation?
- Welche Personengruppen müssen identifiziert werden?
- Welche Werkzeuge stehen zur Verfügung?
„Das also ist des Pudels Kern“, der unter dem Schlagwort der „holistischen Früh- und Hochdurchsatzdiagnostik des InstRadBioBw“ im Folgenden beschrieben wird.
Die Szenarien
Im Rahmen radiologischer (z. B. Freisetzen radioaktiven Materials i.R. eines terroristischen Akts in einem Einkaufszentrum, Bahnhof, Flughafen oder Stadion) oder nuklearer (RN) Szenarien (z. B. Einsatz improvisierter Kernwaffen) werden wenige, dutzende, hunderte oder tausende Individuen betroffen sein. Befördert durch die Massenmedien wird die Strahlenexposition schnell kommuniziert werden. Die Krankenhäuser werden sich auf eine schnell ansteigende und hohe Anzahl möglicherweise und tatsächlich strahlenexponierter Personen vorbereiten müssen. In dieser Situation müssen aus Sicht des InstRadBioBw folgende 3 Personengruppen identifiziert werden:
1. Unbestrahlte Individuen
Sie benötigten keinen Klinikaufenthalt. Ihre Identifikation verhindert den Verbrauch limitierter klinischer Ressourcen. Diese werden für ASK-Patienten benötigt.
2. Gering bestrahlte Individuen
Sie benötigten keinen Klinikaufenthalt. Nach niedrigeren Strahlenexpositionen überleben genetisch veränderte Zellen. Somit treten Spätschäden Jahre und Jahrzehnte nach Bestrahlung (Tumorentwicklung, kardiovaskuläre Erkrankungen) mit höherer Wahrscheinlichkeit auf. Die Identifikation entsprechend Strahlenexponierter ermöglicht eine engmaschigere Überwachung über mehrere Dekaden nach Bestrahlung.
3. Hochbestrahlte Individuen
Bei diesenmanifestiert sich die lebensbedrohliche ASK zeitverzögert. Frühe Hospitalisierung, Bereitstellung von Intensivbetten und früher Therapiebeginn (z. B. Einsatz von Zytokinen) verbessern die Prognose erheblich.
Schlüsselrolle: Frühdiagnostik
Eine Früh- und Hochdurchsatz- sowie eine „point of care“-Diagnostik (die in idealer Weise in den Krankenhäusern vor Ort erfolgen kann) ist erforderlich. Hierzu wurden in verschiedenen wissenschaftlichen Gesellschaften unterschiedliche Werkzeuge entwickelt. Sie werden zur physikalischen, biologischen und klinischen Dosimetrie zusammengefasst. Es besteht breiter Konsens, dass kein Ansatz allein die möglichen unterschiedlichen RN-Szenare abdecken kann.
Der Kern aller diagnostischen Verfahren muss jedoch in der Unterstützung des medizinischen Managements durch Identifikation der beschriebenen Personengruppen liegen.
Seitens des InstRadBioBw favorisieren wir einen Ansatz, bei dem ähnlich den Schichten einer Zwiebel unterschiedliche Ebenen der Komplexität im Gesamtzusammenhang (holistisch) betrachtet werden (Abbildung 1).
Zeitlich betrachtet stellt die
- Strahlenexposition die erste „Schicht“ dar. Daraus erfolgt
- die biologische Prozessierung von Strahlenschäden, aus denen sich
- Biomarker „downstream“ der Exposition mit einer größeren Nähe (und u. U. größeren Relevanz) zum Effekt (ASK Prädiktion) identifizieren lassen. Die Quantifizierung dieser Biomarker zur Prädiktion der ASK muss
- in verständliche klinische Handlungsanweisungen konvertiert werden, damit als Kern des Problems die medizinische Behandlung des Patienten unterstützt werden kann.
Das InstRadBioBw entwickelte zwei Werkzeuge zur Prädiktion der ASK. Diese Werkzeuge konvertieren darüber hinaus zytologische und molekularbiologische Messdaten in klinische Handlungsanweisungen. Im Folgenden werden die genannten vier „Schichten“ sowie die beiden am InstRadBioBw entwickelten Werkzeuge (H-Modul und eine Genexpressionskombination zur Prädiktion der ASK) vorgestellt.
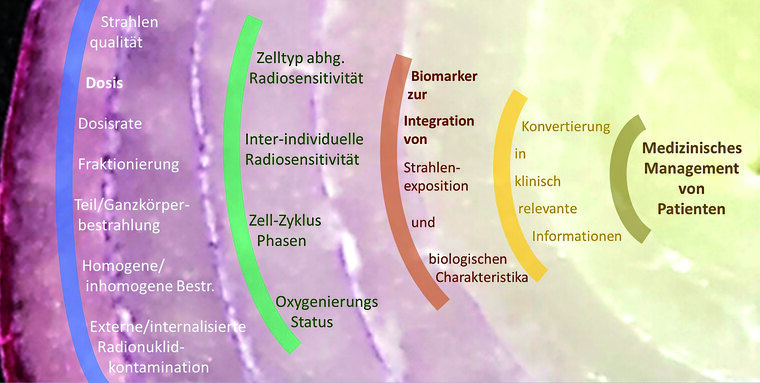
Abb. 1: Darstellung des Konzepts von Biomarkern, die sowohl Charakteristika der Strahlenexposition als auch biologische Faktoren integrieren und deren Werte in klinisch relevante Informationen zum medizinischen Management strahlenexponierter Patienten konvertiert werden. Dieser Ansatz, ähnelt den Schichten einer Zwiebel (Hintergrundbild), indem verschiedene Ebenen der Komplexität im Gesamtzusammenhang (holistisch) betrachtet werden.
Prädiktion von Strahlenschäden
Strahlenexposition ist multidimensional – die Prädiktion gesundheitlicher Effekte ist deshalb schwierig.
Die ASK entwickelt sich aufgrund eines massiven Zelltodes. Konsekutiv erfolgt ein Organfunktionsverlust in Organsystemen mit hohem Zellumsatz, wie im hämatopoetischen, gastrointestinalen, vaskulären und kutanen Systemen. Auch das Nervensystem ist durch Interphasetod und vaskuläre Veränderungen (mit konsekutiver Hirndrucksymptomatik) betroffen. Die Höhe des Zellverlustes bedingt schließlich den Schweregrad der ASK.
Verschiedene Charakteristika der Strahlenexposition tragen wesentlich zum Zelltod bei und sind seit Beginn der Radiobiologie beschrieben worden (Abbildung 1, erste Schicht). So können bei gleicher Dosis nach Neutronenbestrahlung 20mal mehr Zellen sterben im Vergleich zur Bestrahlung mit weniger ionisierenden Gamma-Strahlen gleicher Dosis, aber anderer Strahlenqualität. Zudem stellen Einzel- versus fraktionierte Bestrahlung, homogene versus inhomogene Bestrahlung, Teil- versus Ganzkörperbestrahlung sowie die Dosisrate und die Radionuklidinkorporation weitere Komponenten der Strahlenexposition dar, die entscheidend zum Anteil überlebender Zellen und somit dem Schweregrad der ASK beitragen.
Die Angabe der absorbierten Dosis allein kann deshalb nicht ausreichen, wenn die Prädiktion des Schweregrades der ASK (des Effekts) das diagnostische Ziel sein soll.
Eine Vielzahl biologischer Prozesse entscheidet über das Ausmaß des strahleninduzierten Zelltodes und somit des ASK-Schweregrades.
Zellen und Gewebe reagieren auf die gleiche Strahlenexposition bedingt durch ihre intrinsische Radiosensitivität sehr unterschiedlich (Abb. 1, zweite Schicht). So sind Knochenmark-Stammzellen strahlenempfindlicher als Brust-, Hoden- oder Schilddrüsenzellen. Aus der Radiotherapie sind zudem große Unterschiede in der Nebenwirkungsrate aufgrund inter-individueller Radiosensitivitätsunterschiede bekannt. Zellen, die in unterschiedlichen Zellzyklusphasen bestrahlt werden (Zellen in später S-Phase sind weniger strahlenempfindlich), zeigen große Unterschiede der Überlebensfraktion. Der Oxygenierungsstatus (strahleninduzierte Sauerstoffradikale in oxygenierten Geweben bedingen eine höhere Zelltodesrate) repräsentiert einen weiteren zu berücksichtigenden Aspekt. Deshalb werden hypoxische Zellen mit höherer Wahrscheinlichkeit überleben, als normoxische Zellen. Auch diese Vielzahl biologischer Prozesse gilt es zu berücksichtigen, wenn es um die Prädiktion des ASK Schwergrades geht.
Die Integration von Strahlenexpositions-Charakteristika und strahleninduzierten biologischen Prozesse durch Biomarker ermöglicht eine ASK- Prädiktion.
Strahlenexposition (Abbildung 1, äußere Schicht) führt zu biologischen Änderungen, bei der biologische Prozesse mitberücksichtigt werden müssen (Abbildung 1 , zweite Schicht). Biologische Ereignisse, die downstream dieser Ereignisse stattfinden, haben u. U. das Potenzial der Integration beider Determinanten, die zum ASK-Schweregrad beitragen (Abbildung 1, dritte Schicht). So erlaubt zum Beispiel ein früher Lymphozytenabfall sowie ein kurzfristiger Anstieg und späterer Abfall der Granulozytenanzahl innerhalb der ersten drei Tage nach Bestrahlung eine Prädiktion des Schweregrades der sich später entwickelnden hämatopoetisch geprägten ASK (H-ASK). Die Änderungen der Blutzellzahlen sind auf massiven Zelltod in den Anteilen des Knochenmarks sowie des peripheren Bluts zurückzuführen, die bestrahlt worden sind. Würde lediglich ein Teil des Körpers unterschiedlichen Strahlenqualitäten oder Dosisraten ausgesetzt sein, so würden weniger Zellen sterben, als nach Ganzköperexposition und mit steigender Dosisrate. Die Anzahl überlebender Zellen würde schließlich den H-ARS-Schweregrad und die Ausprägung klinischer Symptome der H-ARS wie Immunsuppression oder Hämorrhagie bedingen. In gleicher Weise würden biologische Faktoren wie inter-individuelle Radiosensitivität berücksichtigt sein.
Kürzlich wurde durch InstRadiBioBw und andere gezeigt, dass die Prädiktion der H-ASK mit Hilfe strahleninduzierter Blutbildveränderungen sowie auf Genexpressions- und Proteinebene gelingen kann (siehe Literaturverzeichnis).
Klinische Anwendung
Konvertierung strahleninduzierter Biomarker-Daten in klinische Handlungsanweisungen
Unter Verwendung biologischer und physikalischer Dosimetrieverfahren entwickelte sich die dominierende Vorstellung, dass eine Abschätzung der Dosishöhe zur Prädiktion der ASK ausreichend sei. Wie zuvor dargestellt, ist dieser Ansatz aber übersimplifiziert und greift viel zu kurz. Er ist zudem für Personen, die mit dem in der Radiobiologie gebräuchlichen Dosiskonzept nicht vertraut sind, schwer nachvollziehbar. Wichtige und entscheidende Begriffe wie Radioaktivität, absorbierte Dosis, Äquivalent- und Effektiv-Dosis sowie assoziierte Dimensionen wie Becquerel, Gray und Sievert komplizieren das Verständnis. Diese Situation ähnelt dem hypothetischen Dialog eines Arztes mit einem an Corona infizierten Patienten: Statt Symptome, Symptomschwere und Krankheitsverlauf zu erfassen, würde der Arzt aus der Anzahl der Viren zu Beginn der Infektion (der Expositionshöhe in Analogie zur Dosisabschätzung) das therapeutische Procedere ableiten.
Offensichtlich müssen strahleninduzierte Änderungen, z. B. des peripheren Blutbildes oder Änderungen der Kopienanzahl bestimmter Gene, in klinisch relevante Informationen konvertiert werden. Dies wurde für das am InstRadBioBw entwickelte H-Modul (Abbildung 2) und einer Genexpressionskombination (Abbildung 3) zur H-ASK-Prädiktion realisiert und wird in den folgenden beiden Kapiteln vorgestellt werden.

Abb. 2: Blutbildveränderungen (Änderung der Lymphozyten-/Granulozyten-/Thrombozytenanzahl) nach Bestrahlung stellen ein Beispiel integrierender Biomarker zur ASK-Prädiktion dar. Es entstand hieraus die sogenannte Online-App „H-Modul‟.
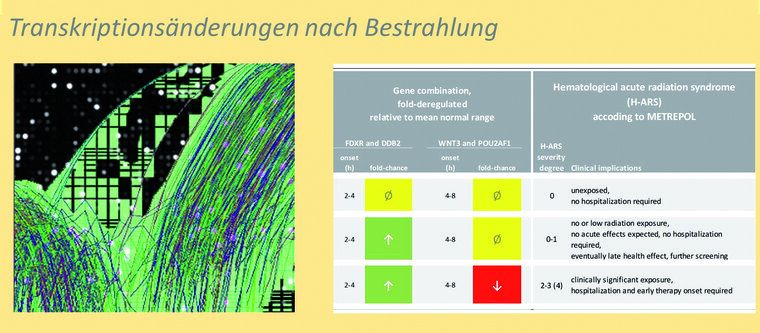
Abb. 3: Das InstRadBioBw entwickelte eine Genexpressionskombination zur Vorhersage der hämatologischen ASK als zweites Beispiel für den Einsatz integrierender Biomarker zur ASK-Prädiktion.
H-Modul
In vorangegangenen Studien untersuchte das InstRadBioBw strahleninduzierte Änderungen der Anzahl peripherer Blutbestandteile zur Prädiktion der H-ARS-Schweregrade überwiegend an Daten von tatsächlichen Strahlenunfallopfern. Mathematische Modelle (logistische Regressionsanalyse) wurden verwendet, um an 454 Blutbildern von 267 Personen die nach den Medical Treatment Protocols for Radiation Accident Victims (METREPOL) definierten Schweregrade der H-ASK zu korrelieren.
Diese Schweregrade (H-ASK 0–4 gem. METREPOL) dienen als Informationsquelle für Ärzte. Jeder Schweregrad impliziert eine klinische Behandlungsempfehlung. Daher erhalten Ärzte bei der Umwandlung von Differentialblutbild-Änderungen in diese Schweregrade automatisch klinische Diagnose- und Behandlungsinformationen. Die Validierung der Modelle wurde an weiteren 275 Differenzialblutbildern von 252 Personen durchgeführt. Die H-ASK-Schweregrade sowie die Differenzialblutbilder stammten bei tatsächlicher Exposition gegenüber ionisierender Strahlung, u. a. von Strahlenunfallopfern, und wurden in der Datenbank SEARCH (System zur Auswertung und Archivierung von Strahlenunfällen basierend auf Fallgeschichten), gespeichert.
In unserer Analyse konzentrierten wir uns auf die Identifikation der zuvor genannten drei Personengruppen, die entsprechend des H-ASK-Schwergrades als H0 (unbestrahlt), H1 (gering bestrahlt) und H2–4 (potenzieller H-ASK-Patient) definiert sind. Die Prädiktion des Schweregrades innerhalb der ersten drei Tage nach der Bestrahlung und vor dem Einsetzen der Krankheitsmanifestation erlaubt den effizienten Einsatz limitierter klinischer Ressourcen für jene, die sie benötigen (H2–4 HARS) und kann zur Beruhigung der anderen involvierten Personengruppen („worried well“) beitragen. Wir zeigten, dass die Prädiktion basierend auf Blutbildveränderungen mit unserem Werkzeug innerhalb des diagnostischen Zeitfensters der ASK von ca. 3 Tagen funktionierte.
Ermutigt durch diese Ergebnisse entwickelten wir eine Reihe von Vorhersagemodell-Tabellen in Microsoft® Excel. Nach Eingabe der Lymphozyten-, Granulozyten oder Thrombozytenanzahl, die innerhalb der ersten 3 Tage nach Bestrahlung zur Verfügung stehen, werden automatisch diagnostische Vorhersagen und therapeutische Empfehlungen generiert (Abbildung 2). Diese Tabellenkalkulationen erwiesen sich in zwei Table-Top-Übungen als nützlich, jedoch wurden auch einige Limitierungen deutlich. Deshalb wurde die Excel-Version des H-Moduls schließlich in eine App umgewandelt. Statt der Befüllung von neun Excel-Tabellen (erforderlich, um unterschiedliche Kombinationen täglicher Differenzialblutbilder widerzuspiegeln und akute/chronische Infektionen als Störfaktor der Differenzialblutbilder zu berücksichtigen), integriert die H-Modul-App diese Eingaben auf einem Bildschirm. Die neue Architektur der App und ihre Funktionsweise wurde kürzlich veröffentlicht (siehe Literaturverzeichnis). Seit Juni 2021 kann diese App über den Apple App Store und den Android Play Store heruntergeladen werden.
Strahlungsinduzierte Genexpressionskombinationen zur H-ASK Prädiktion
Wir identifizierten kürzlich eine Kombination von vier Genen (WNT3, POU2AF1, FDXR und DDB2), die innerhalb von 1–2 Tagen nach Strahlenexposition im peripheren Blut bestrahlter Tiere exprimiert wurden und mit dem H-ASK-Schweregrad korrelierten. Diese Gene wurden anschließend an bestrahlten Tumorpatienten sowie in aufwendigen in vitro Untersuchungen validiert. Die Analyse der Veränderungen in der Expression dieser Genkombination ermöglichte es, zwischen strahlenexponierten Personen, die einen milden H-ASK Schweregrad entwickelten, und solchen, die einen schwereren H-ASK-Grad entwickelten, zu unterscheiden.
Paarweise redundante Gene (FDXR/DDB2 und WTNT3/POU2AF1) mit gleicher Assoziation zu H-ASK-Schweregraden wurden eingesetzt, um die Robustheit der Genkombination zu erhöhen (z. B. Schwierigkeiten mit niedriger Baseline, siehe Abbildung 3).
Die vorgeschlagene Genkombination konvertiert Genexpressionsänderungen in folgender Weise in klinisch relevante H-ASK Kategorien:
- Zur Identifizierung von H-ASK 0 (unbestrahlte Individuen) liegen Änderungen der Kopienanzahl aller vier Gene unter dem zweifachen einer unbestrahlten Referenz. Bis zu zweifache Unterschiede der Genexpression werden zur Anpassung an die methodische Varianz betrachtet und damit als unbestrahlte Individuen interpretiert.
- Zur Identifizierung von H-ASK 1 wird eine > 2-fache Hochregulierung von FDXR und DDB2 und keine Genexpressionsänderungen von WNT3 und POU2AF1 außerhalb der methodischen Varianz (Faktor 2) erwartet.
- Zur Identifizierung von H-ASK 2–4 wird eine > 2-fache Hochregulierung von FDXR und DDB2 und eine ausgeprägte Herunterregulierung von WNT3 und POU2AF1 erwartet.
Basierend auf derzeit verfügbaren Daten sagt eine 10-fache Herunterregulierung von WNT3 oder POU2AF1 den H-ASK Schweregrad 2–4 mit einem positiven Vorhersagewert (positive predictive value, PPV) von 100 % voraus. Eine > 2- und < 10-fache Herunterregulierung von WNT3/POU2AF1 reduziert den PPV von 100 % auf etwa 90 %.
Fazit und „Way Ahead“
Die Identifizierung von Biomarkern zur ASK-Prädiktion sowie die Konvertierung von Biomarkerdaten in leicht nachvollziehbare klinische Informationen erscheint vielversprechend. Zukünftige Arbeiten zur Validierung der entwickelten Instrumente sowie deren Weiterentwicklung, z. B. unter Einsatz künstlicher Intelligenz, werden folgen müssen. Zudem erfassen die entwickelten Werkzeuge andere lebensbedrohliche Syndrome der ASK wie z. B. das gastrointestinale Syndrom nicht. Ein weiteres Ziel liegt in der Verbreitung und Schulung der entwickelten Werkzeuge mit Hilfe verschiedener Plattformen. Hierzu gehören u. a. die Durchführung von Workshops (NATO StTARS workshop) und die Unterrichtung von Radiobiologiestudenten des Masterstudiengangs Radiobiologie der Technischen Universität München.
Literaturhinweise
- Blakely WF, Bolduc DL, Debad J, Sigal G, Port M, Abend M et al.:Use of Proteomic and Hematology Biomarkers for Prediction of Hematopoietic Acute Radiation Syndrome Severity in Baboon Radiation Models. Health Phys. 2018; 115(1): 29–36. mehr lesen
- Hall EJ, Giaccia AJ: Radiobiology for the Radiologist: Seventh Edition, 2012.
- Majewski M, Rozgic M, Ostheim P, Port M, Abend M: A New Smartphone Application to Predict Hematologic Acute Radiation Syndrome Based on Blood Cell Count Changes-The H-module App. Health Phys. 2020; 119(1): 64-71. mehr lesen
- Port M, Hérodin F, Drouet M, Valente M, Majewski M, Ostheim P et al.: Gene expression changes in irradiated baboons - a summary and interpretation of a decade of findings. Radiat Res. 2021; 195(6): 501-521. mehr lesen
- Port M, Pieper B, Dörr HD, Hübsch A, Majewski M, Abend M: Correlation of Radiation Dose Estimates by DIC with the METREPOL Hematological Classes of Disease Severity. Radiat Res. 2018; 1: RR14936.1. mehr lesen
- Port M, Majewski M, Herodin F et al.: Validating Baboon Ex Vivo and in Vivo Radiation-Related Gene Expression with Corresponding Human Data. Radiat Res [Internet] 2018; 189(4): 389–398. mehr lesen
- Port M, Pieper B, Knie T et al.: Rapid Prediction of Hematologic Acute Radiation Syndrome in Radiation Injury Patients Using Peripheral Blood Cell Counts. Radiat Res. 2017; 188(2): 156–168. mehr lesen
- Port M, Herodin F, Valente M et al.: First Generation Gene Expression Signature for Early Prediction of Late Occurring Hematological Acute Radiation Syndrome in Baboons. Radiat Res. 2016; 186(1): 39–54. mehr lesen
Für die Verfasser
Oberstarzt Prof. Dr. Michael Abend (M. Sc.)
Institut für Radiobiologie der Bundeswehr
Neuherbergstr. 11, 80937 München
E-Mail: michaelabend@bundeswehr.org